2025年,欧盟新型食品(Novel Food)监管延续审慎基调,无论是欧洲食品安全局(EFSA)发布的科学意见,还是Union List在官方公报层面的更新,都显示出欧盟正通过更精细的条件设定与分类管理,引导创新原料有序进入市场。

ZMUni中贸合规中心对2025年欧盟新型食品(Novel Food)的相关情况进行了梳理与总结,旨在为行业从业者提供参考。
01.
2025年欧盟新型食品情况
🌟申请状况
数量及种类方面:
根据欧洲食品安全局(EFSA)的数据统计:
🔶2025年共接受47份新型食品申请卷宗(Dossier received),相较于2024年(62份)有所下降。2025年接受的卷宗中:
🔸42份为新型食品申请(Novel Food Application)
🔸5份为传统食品通报/ 申请(Traditional Food Notification/ Application)
2025年接收的申请卷宗进展(状态)方面:
🔶5份申请被判定为无效(Application Not Valid)
🔶不足3成的申请已开始风险评估(Ongoing Risk Assessment)
🔶2份申请风险评估已结束,EFSA科学意见(Scientific Opinion)已发表(Published)
🌟EFSA科学意见发布情况
2025年,欧洲食品安全局(EFSA)共发布了28份新型食品科学意见(安全评估报告),较2024年的11份有显著增加。
以下为2025年EFSA已发布科学意见的新型食品申请一览:

🌟新型食品目录(the Union List)变动
2025年,《欧盟官方公报》(OJEU)
🔶对7款新型食品进行了修订
🔸使用条件、质量规格、标签标识变更等
🔶新授权了10款新型食品申请
🔸含1款第三国传统食品
较2024年的9款修订,13款新授权均有所回落。
获得新授权的10款新型食品的信息如下:
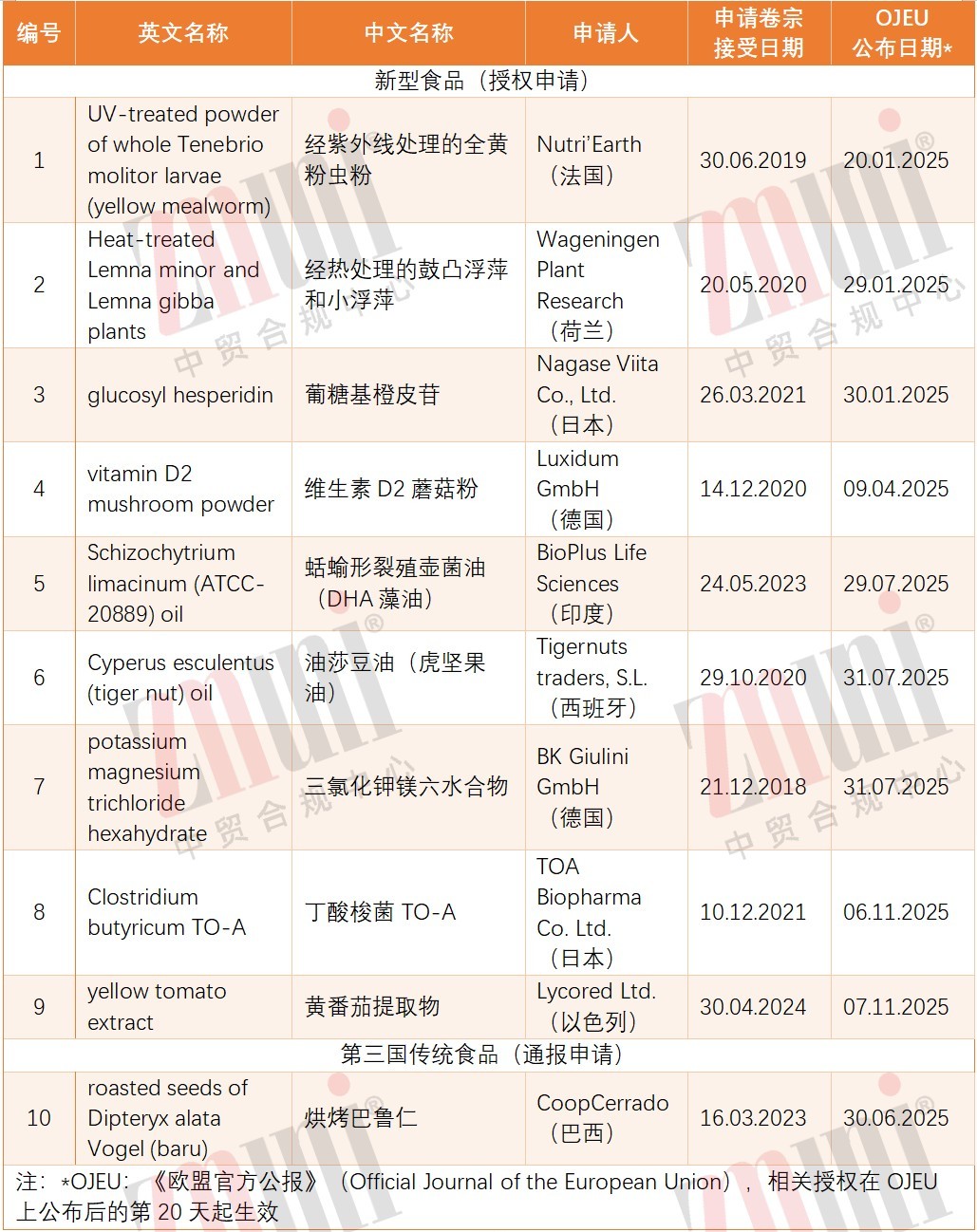
02.
✊️ 合规启示✊️
从2025年的授权与修订情况看,欧盟新型食品审评在“物质层面”呈现以下特征:一是对来源清晰、加工路径明确、成分界定清楚的物质,更容易在现有框架下获得授权或完成修订;二是涉及发酵产物、提取物或功能性成分时,审评仍会趋于审慎,往往需要申请人提供更加全面的安全性论证资料。
在“周期层面”,2025年的数据进一步表明,新型食品的审批过程并非快速准入机制。从卷宗准备与提交、欧洲食品安全局科学评估,到最终列入许可清单,整体所需时间仍主要取决于卷宗质量。补正程序依旧是影响审批周期的重要因素,多数延迟并非源于监管收紧,而与企业前期准备不充分有关。相比之下,对已授权新型食品的修订程序在时间可控性和监管可预期性方面,通常更具优势。
基于以上观察,【ZMUni中贸合规中心】建议申报企业在决策时保持理性预期:在物质选择上,优先考虑其在欧盟监管体系中的定位可行性;在时间规划上,应将新型食品申报纳入中长期市场策略,而非视为短期上市手段。【ZMUni中贸合规中心】认为,选择适宜的物质、设定合理的用途范围,并对时间成本形成清晰预估,仍是在目前监管环境下,降低申报风险的最务实路径。
