ZMUni中贸合规中心整理了2026年第一季度欧盟新型食品的相关情况,供大家参考。
更多欧盟Novel Food往期文章:
EFSA评估结果(3例)
1️⃣ 6′-唾液酸乳糖(6′-SL)钠盐
|
英文名称 |
6′-sialyllactose (6′-SL) sodium salt produced with a derivative strain (Escherichia coli K-12 MG1655 INB-6SL_02) of E. coli K-12 MG1655 (ATCC 700926) |
|
申请人 |
Inbiose N.V.(比利时) |
|
申请卷宗 接收日期 |
2023-10-30 |
|
生产工艺 |
合成生物学来源:由大肠埃希菌(Escherichia coli)K-12 MG1655(ATCC 700926)的衍生菌株Escherichia coli K-12 MG1655 INB-6SL_02生产 |
|
质量规格👇 |
|
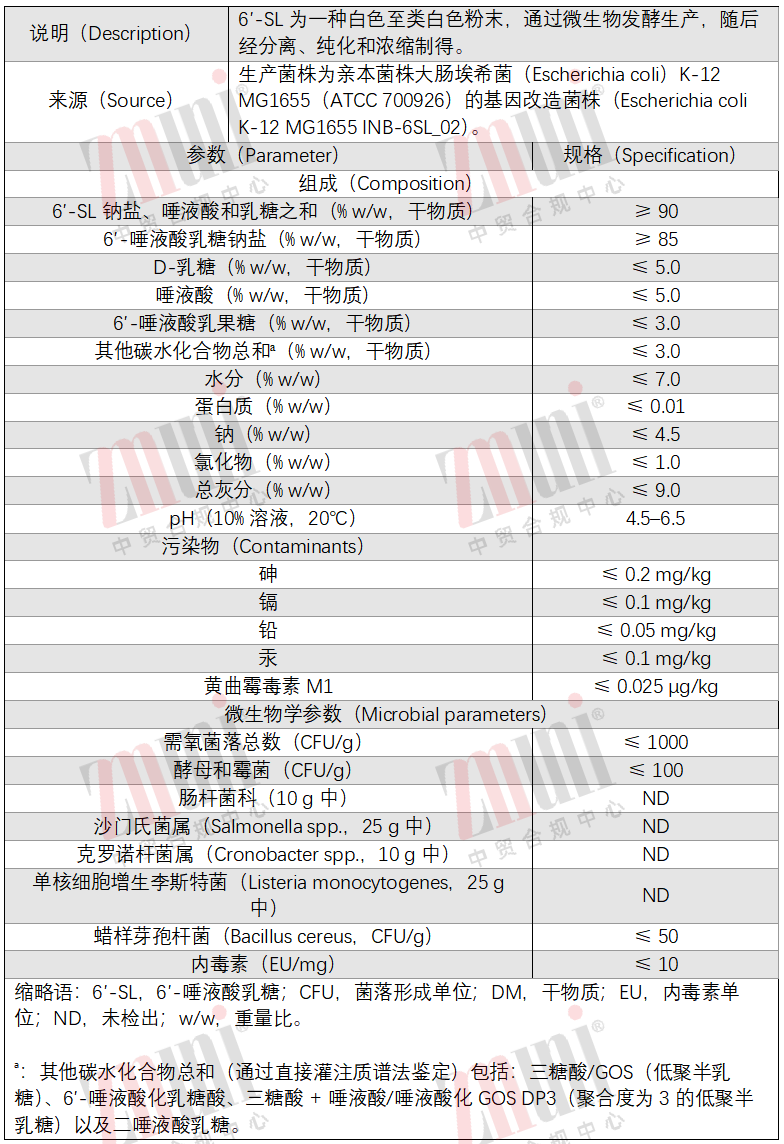 |
|
|
申请人拟定使用条件👇 |
|
|
根据申请人提交的信息,本次申请中的6′-唾液酸乳糖(6′-SL)钠盐并不拟调整目前已获授权的使用范围和使用水平,仍沿用此前针对“微生物来源”6′-SL 钠盐已批准的使用条件和添加量。即该产品拟定的用途、使用食品类别及相应使用量与现有授权内容保持一致,不涉及新增用途或提高使用水平。 在适用人群方面,申请人拟定的目标人群为一般人群。不过,对于食品补充剂(Food Supplement, FS)产品,其适用对象限定为3岁以上人群。 在使用限制方面,申请人拟采用与其他生产工艺所得同类产品一致的限制条件,即:FS不适用于婴儿和幼儿;同时,如在同一天内已经食用了其他添加 6′-SL 钠盐的食品,则不应再食用该类FS产品。 |
|
|
EFSA评估意见👇 |
|
|
EFSA 专家组认为,该新食品(NF)主要由 6′-唾液酸乳糖(6′-SL)钠盐 以及其他结构相关的单糖和低聚糖组成。根据申请材料、产品特性及拟定使用条件的综合评估,专家组得出结论:该新食品在申请人提出的使用条件下是安全的。 |
|
2️⃣ 3′-唾液酸乳糖钠盐(3′‐SL)
|
英文名称 |
3′‐sialyllactose (3′‐SL) sodium salt produced with a derivative strain (Escherichia coli K‐12 MG1655 INB‐3SL_01) of E. coli K‐12 MG1655 (ATCC 700926) |
|
申请人 |
Inbiose N.V.(比利时) |
|
申请卷宗 接收日期 |
2024-01-03 |
|
生产工艺 |
合成生物学来源:由大肠埃希菌(Escherichia coli)K-12 MG1655(ATCC 700926)的衍生菌株Escherichia coli K-12 MG1655 INB-3SL_01生产 |
|
质量规格👇 |
|
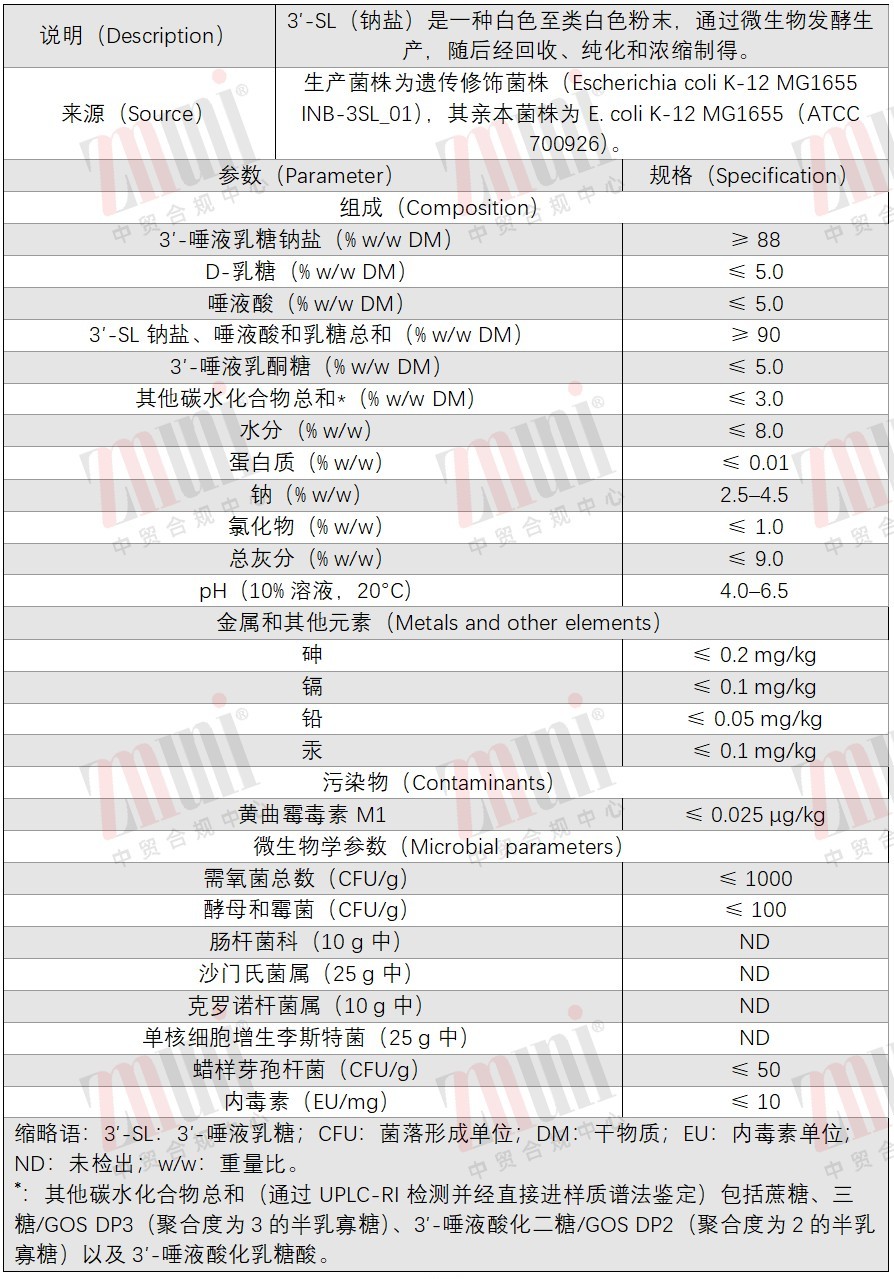 |
|
|
申请人拟定使用条件👇 |
|
|
根据申请人提交的信息,本次申请中的3′-唾液酸乳糖(3′-SL)钠盐并不拟调整目前已获授权的使用范围和使用水平,仍沿用此前针对“微生物来源”3′-SL钠盐已批准的使用条件和添加量。即,该新食品拟定的用途、适用食品类别及相应使用量与现有授权内容保持一致,不涉及新增用途或提高使用水平,因此其预期摄入程度亦与已授权的3′-SL钠盐相当。 在适用人群方面,申请人拟定的目标人群为一般人群。不过,对于食品补充剂(Food Supplement, FS)产品,其适用对象限定为3岁以上人群。 在使用限制方面,申请人拟采用与其他生产工艺所得同类产品一致的限制条件,即:FS不适用于婴儿和幼儿;同时,如在同一天内已经食用了其他添加3′-SL钠盐的食品,则不应再食用该类FS产品。 |
|
|
EFSA评估意见👇 |
|
|
EFSA专家组认为,该新型食品(NF)由3′-SL(钠盐)及其他结构相关的单糖和低聚糖组成,在拟议的使用条件下是安全的。 |
|
3️⃣ 大麻二氧化碳提取物
|
英文名称 |
carbon dioxide extract from Cannabis sativa L. |
|
申请人 |
Charlotte's Web, Inc.(美国&加拿大) |
|
申请卷宗 接收日期 |
2021-04-22 |
|
生产工艺 |
其工艺路线主要包括两种来源:从工业大麻中提取CBD,或通过化学合成制得CBD;随后将高纯度CBD进一步纯化并配制成油基食品补充剂制剂(天然提取&化学合成) |
|
质量规格 |
申请人提出了该新食品(NF)的质量规格。然而,由于EFSA意见的最终结论,这些质量规格未予报告。 |
|
申请人拟定使用条件👇 |
|
|
申请人拟将该新食品(NF)用于食品补充剂。目标人群为3岁以上一般人群,但不包括孕妇和哺乳期妇女。根据申请人提出的使用方案,含该新食品的最终制剂针对不同预期人群设定了不同的最大日摄入量,范围为34–109 mg/天;其中,最终制剂中该新食品(工业大麻提取物)的添加比例为3.3%。此外,根据组成资料,该新食品除CBD外还含有其他大麻素成分,但申请人未就这些其他大麻素开展暴露评估。 |
|
|
EFSA评估意见👇 |
|
|
EFSA在本次更新评估意见中认为,现有证据仍不足以消除CBD作为新食品的关键安全性疑虑。尽管自2022年首次声明以来新增了不少研究,但多数研究仍存在试验周期短、方法学不统一及合并用药干扰等局限,尚不足以填补既有数据缺口。综合动物实验、人体研究以及申请材料中的90天毒理数据,EFSA认为肝脏仍是CBD最敏感且最一致受影响的靶器官,同时对神经系统、生殖与发育、内分泌及免疫相关风险仍持谨慎态度。在此基础上,EFSA通过基准剂量法提出了一个临时安全剂量,即0.0275 mg/kg体重/天(约相当于70 kg成年人每日2 mg),但这一数值仅适用于纯度不低于98%、生产工艺被认为安全、已排除遗传毒性且不涉及小颗粒或纳米颗粒暴露的食品补充剂型CBD制剂。总体而言,EFSA并未确认CBD新食品的广泛食用安全性,特别是对于25岁以下人群、孕妇和哺乳期妇女,以及合并用药人群,其安全性仍无法建立。 |
|
EFSA提供的科学和技术支持(1例)
EFSA更新CBD新型食品安全声明:审评口径未放松,安全结论仍然审慎
欧洲食品安全局(EFSA)近日发布《关于大麻二酚(CBD)作为新型食品安全性的更新声明》,对其2022年声明之后新增的科学证据进行了系统审查。整体来看,这份文件并未改变欧盟监管部门此前的基本判断:在现阶段证据条件下,CBD作为新型食品的安全性仍无法被充分确认,相关审评口径总体保持审慎。
从文件定位看,此次更新并非对CBD作出授权判断,而是对既有风险认识进行再梳理,重点回答两个问题:一是2022年识别出的关键数据缺口是否已被新研究填补;二是现有证据能否支持进一步明确CBD的安全暴露边界。EFSA的结论较为明确:虽然近几年相关研究数量增加,但多数新增研究仍存在样本量有限、观察周期较短、试验设计不统一、受试者合并用药等局限,尚不足以实质性消除前期不确定性。
从监管关注重点看,肝脏风险仍是本轮评估的核心。EFSA指出,动物研究中,肝重增加及组织病理学变化持续表现为较敏感终点;人体研究中,也观察到部分受试者在摄入CBD后出现转氨酶升高,提示其具有潜在肝毒性,且在与其他药物共同使用时风险可能上升。对监管而言,这意味着CBD并不适合被简单理解为“低风险天然成分”,其安全评估仍需围绕明确的毒理学终点展开。
除肝脏外,EFSA此次也继续维持对胃肠道、神经精神系统、内分泌系统以及生殖和发育毒性的关注。文件显示,较高剂量CBD摄入与腹泻、呕吐等胃肠道不良反应有关;神经、精神和心理方面的数据仍明显不足,尤其缺乏针对健康人群、长期暴露和剂量反应关系的可靠资料;动物研究则进一步强化了对生殖毒性、胎儿发育和神经发育影响的担忧。与此同时,CBD对多种药物代谢酶具有抑制作用,提示其可能改变合并用药的体内暴露水平,这也是监管部门持续强调的重要风险点。
值得关注的是,EFSA在本次文件中首次基于符合规范的90天动物研究进行了基准剂量建模,并提出了一个临时安全剂量。按文件计算结果,该数值为0.0275 mg/kg体重/天,折算后约相当于70公斤成年人每日2 mg CBD。但从监管适用范围看,这一数值具有明显前提条件:仅适用于纯度不低于98%的CBD食品补充剂制剂,且需满足生产工艺可接受、已排除基因毒性、并不涉及纳米颗粒等条件。因此,这一数值更应理解为在严格限定条件下形成的审评参考点,而非对市场上各类CBD口服产品的普遍安全背书。
从欧盟监管实践看,这份更新声明释放出的信号比较清晰。第一,CBD新型食品审评门槛并未降低。文件显示,截至2025年8月,欧盟已收到200多份CBD新型食品申请,但口服CBD产品在欧盟现行新型食品框架下仍未获得授权;目前欧盟市场上唯一获批的CBD产品仍是处方药Epidyolex/Epidiolex,而非普通食品或保健品。第二,监管关注点进一步聚焦于长期暴露和特殊人群风险。EFSA明确表示,基于现有数据,25岁以下人群、孕妇、哺乳期女性以及正在同时服药的人群,其CBD食用安全性仍无法建立。
对企业而言,这意味着今后CBD新型食品申报不能依赖零散、短期或治疗场景下的人体试验来支撑一般食品用途安全性。围绕长期摄入、肝毒性、生殖与发育毒性、神经系统影响、药物相互作用以及纳米颗粒相关问题,申请人仍需提交更完整、更规范、与目标消费场景更匹配的证据材料。尤其是对于拟作为食品补充剂销售的产品,剂量设定、适用人群界定、产品纯度和工艺控制都将成为实质审评重点。
对市场而言,这份文件也意味着,当前不少商业宣传中将CBD描述为“天然、安全、可长期日常服用”的表达,与欧盟风险评估结论之间存在明显张力。就现有证据看,监管部门并未给出宽松结论,反而以更保守方式划定了当前科学证据所能支持的边界。总体而言,EFSA此次更新并不是放行信号,而更接近于一次风险重点重申:在关键数据缺口未补齐之前,CBD作为新型食品的合规路径仍将处于高审慎状态。
上下滑动阅读完整内容
授权条例发布(3例)
1️⃣新授权
|
(1) 乳糖-N-四糖(Escherichia coli K-12 MG1655 (ATCC 700926)来源) |
|
|
英文名称 |
lacto-N-tetraose produced by a derivative strain of Escherichia coli K-12 MG1655 (ATCC 700926) |
|
申请人 |
Inbiose N.V.(比利时) |
|
授权条例 |
Commission Implementing Regulation (EU) 2026/397 of 23 February 2026 authorising the placing on the market of lacto-N-tetraose produced by a derivative strain of Escherichia coli K-12 MG1655 (ATCC 700926) as a novel food and amending Implementing Regulation (EU) 2017/2470 |
|
OJEU 公布日期 |
2026.02.23 |
|
(2) 脱脂油菜籽粉 |
|
|
英文名称 |
defatted rapeseed powder |
|
申请人 |
NapiFeryn BioTech Sp. z o.o.(波兰) |
|
授权条例 |
Commission Implementing Regulation (EU) 2026/386 of 20 February 2026 authorising the placing on the market of defatted rapeseed powder as a novel food and amending Implementing Regulation (EU) 2017/2470 |
|
OJEU 公布日期 |
2026.02.20 |
2️⃣修订
|
(1)嗜黏蛋白阿克曼菌(经巴氏杀菌) |
|
|
英文名称 |
pasteurised Akkermansia muciniphila |
|
申请人 |
Akkermansia Company SA(比利时) |
|
授权条例 |
Commission Implementing Regulation (EU) 2026/391 of 23 February 2026 amending Implementing Regulation (EU) 2017/2470 as regards the conditions of use and the specific labelling requirements of the novel food pasteurised Akkermansia muciniphila |
|
OJEU 公布日期 |
2026.02.23 |
|
修订内容👇 |
|
|
🟠主要集中在使用条件、标签要求和授权持有人信息三个方面: 🔸原授权范围仅限于成年人使用的食品补充剂和特殊医学用途食品,此次修订后,使用人群扩大至12岁以上未满18岁的一般人群;其中,12岁以上人群的最大使用量为2.1×10^10 个细胞/天**,14岁以上人群可提高至3.0×10^10 个细胞/天,成年人仍可使用至3.4×10^10 个细胞/天。 🔸孕妇和哺乳期妇女仍被排除在适用范围之外,因为 EFSA 认为其安全性尚不能确定。其次,文件相应调整了特定标签要求:含该新型食品的食品补充剂必须注明,不应由孕妇、哺乳期妇女以及低于相应年龄门槛的人群食用,并应根据产品面向的年龄组分别标示“12岁以下”“14岁以下”或“18岁以下”限制。 🔸文件还将原授权持有人的名称更新为 the Akkermansia Company SA。 |
|
信息来源:
· 欧洲食品安全局(EFSA)
· 《欧盟官方公报》(Official Journal of the European Union)
