美国食品药品监督管理局(FDA)设立的GRAS(Generally Recognized As Safe,即“普遍认为安全”)制度,是全球食品配料行业评估物质安全性的重要参照标准。企业可以通过提交GRAS通知,向FDA展示某一成分基于科学程序在特定用途下的安全性。获得FDA“无异议(No Questions)”回应,意味着该物质的GRAS地位得到了FDA确认,可合法在美国市场中作为食品成分广泛应用。
值得注意的是,FDA GRAS通知数据库并非实时更新,可能存在一定时间的滞后。而在2025年6月10日,FDA对其GRAS数据库进行了新一轮的内容更新。此次更新中,由中国弈柯糖生物科技(上海)有限公司(Adorvia Biotechnology Co., Ltd.)提交的GRAS通知(编号GRN 1206)正式对外公布,显示其瑞鲍迪苷M(Rebaudioside M)已获得FDA确认的GRAS资格。

物质概况
🟠原料名称:通过对从甜叶菊(Stevia rebaudiana(Bertoni)Bertoni)叶中提取纯化的瑞鲍糖苷 A 进行酶处理所生产的瑞鲍糖苷 M。(Rebaudioside M produced by enzymatic treatment of rebaudioside A purified from the leaves of Stevia rebaudiana (Bertoni) Bertoni)
🟠GRAS通知编号:GRN 1206
🟠FDA回函状态:No Questions(无异议)
🟠回函时间:2025年2月28日
🟠预期用途:作为甜味剂,通用于食品(婴儿配方奶粉及肉类、禽类产品除外),使用量依据良好生产规范(GMP)确定
该通告显示,该成分的GRAS认定是基于科学程序提交的完整数据评估。




瑞鲍迪苷简介
Rebaudioside M是从甜叶菊(Stevia rebaudiana)叶中提取的高纯度甜味成分。相较于传统的甜叶菊糖苷(如Reb A),Reb M具有更接近蔗糖的风味,后苦味更轻,口感更顺滑。GRN 1206中的Reb M是通过对Rebaudioside A进行酶促转化制备而成,这种酶法生产方式使得该成分在纯度与一致性方面更具优势。

申请人信息
🟠公司名称:中国弈柯莱生物子公司-弈柯糖生物科技(上海)有限公司(Adorvia Biotechnology Co., Ltd.)
🟠公司地址:中国上海市紫月路1299号3号楼5层,邮编200241
🟠公司背景:弈柯糖生物成立于2024年2月,公司致力于成为全球领先的天然减糖解决方案供应商。是一家专注于生物技术和功能性食品配料研发的企业,致力于通过先进的酶催化与发酵技术,推动天然健康食品成分的产业化发展。
此次申请GRN 1206反映了Adorvia在高纯度甜味剂领域的技术积累与国际市场战略。

国际法规状态
🐉中国
《食品安全国家标准 食品添加剂使用标准》(GB 2760)中已经列明甜叶菊糖苷作为合法的食品添加剂使用。
国家卫生健康委员会(卫健委)于2024年第2号公告中批准甜菊糖苷(酶转换法)为食品添加剂新品种。其为以甜叶菊(Stevia Rebaudiana Bertoni) 叶来源的瑞鲍迪苷 A(Rebaudioside A)为原料, 通过蔗糖合成酶、 β-1,3-糖基转移酶和β-1,2-糖基转移酶高效催化后, 再经醇溶、 过滤结晶、 干燥制得的富含瑞鲍迪苷 M (瑞鲍迪苷 M(以干基计)≥95%)的食品添加剂甜菊糖苷( 酶转化法)。
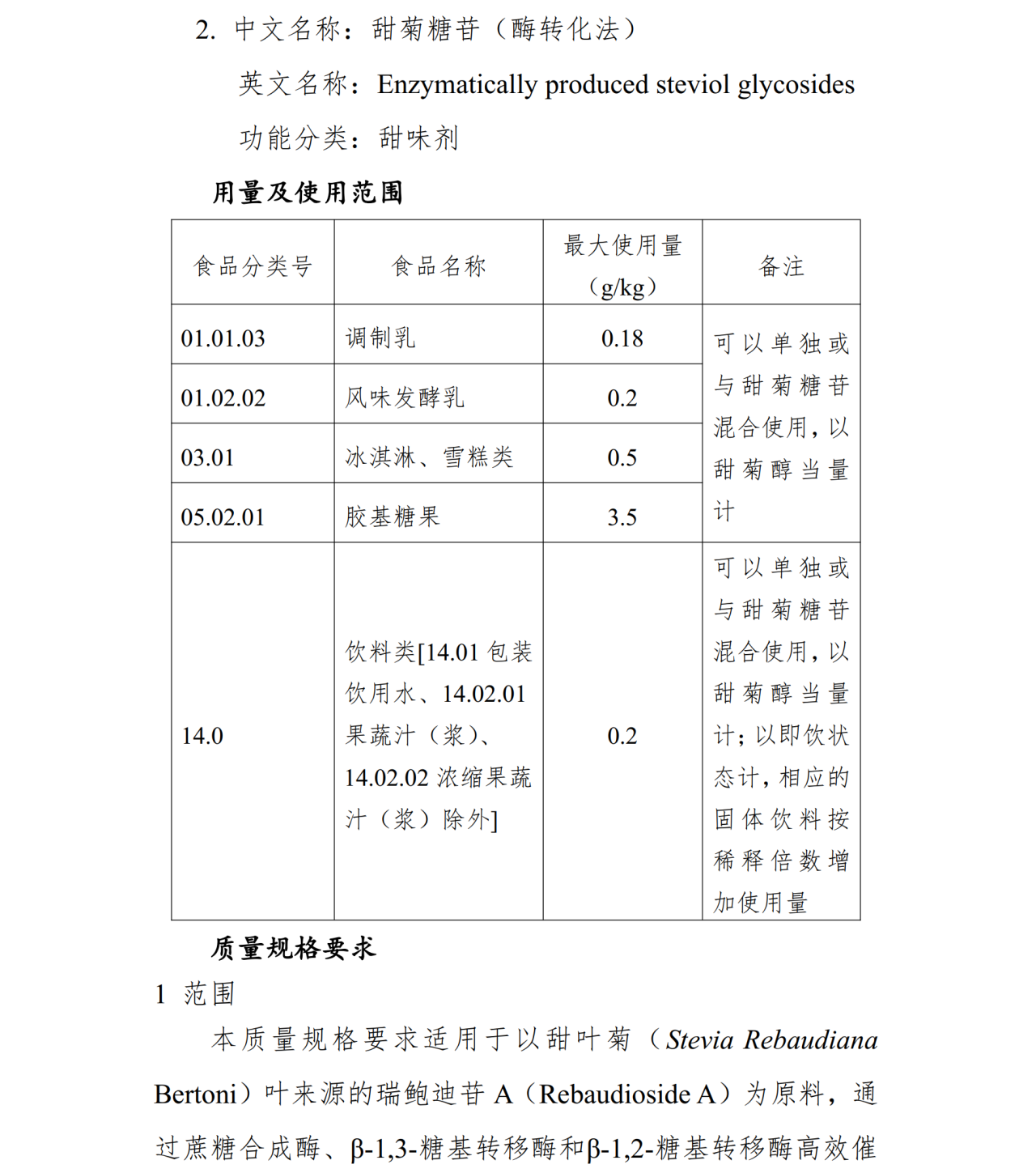
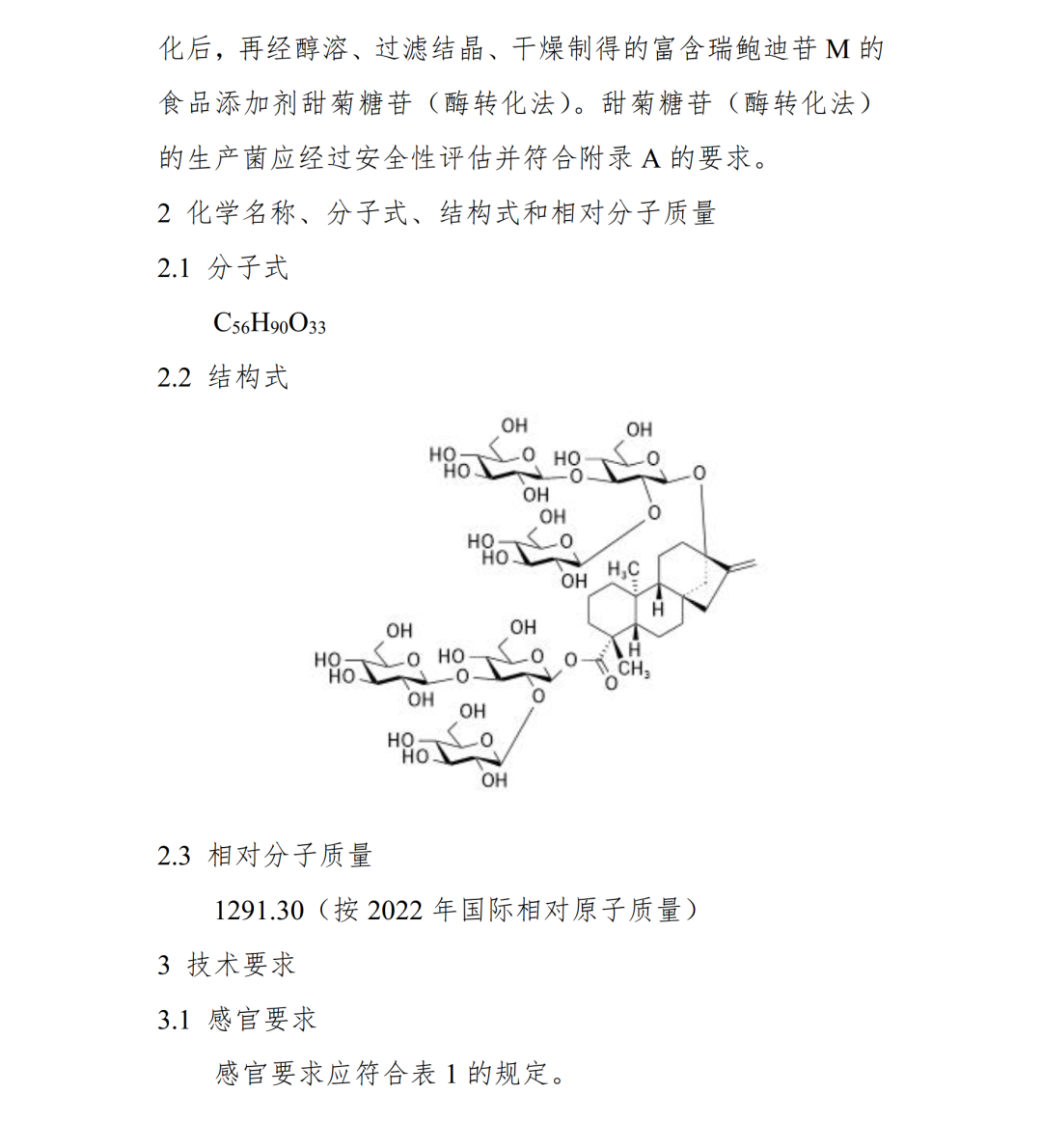
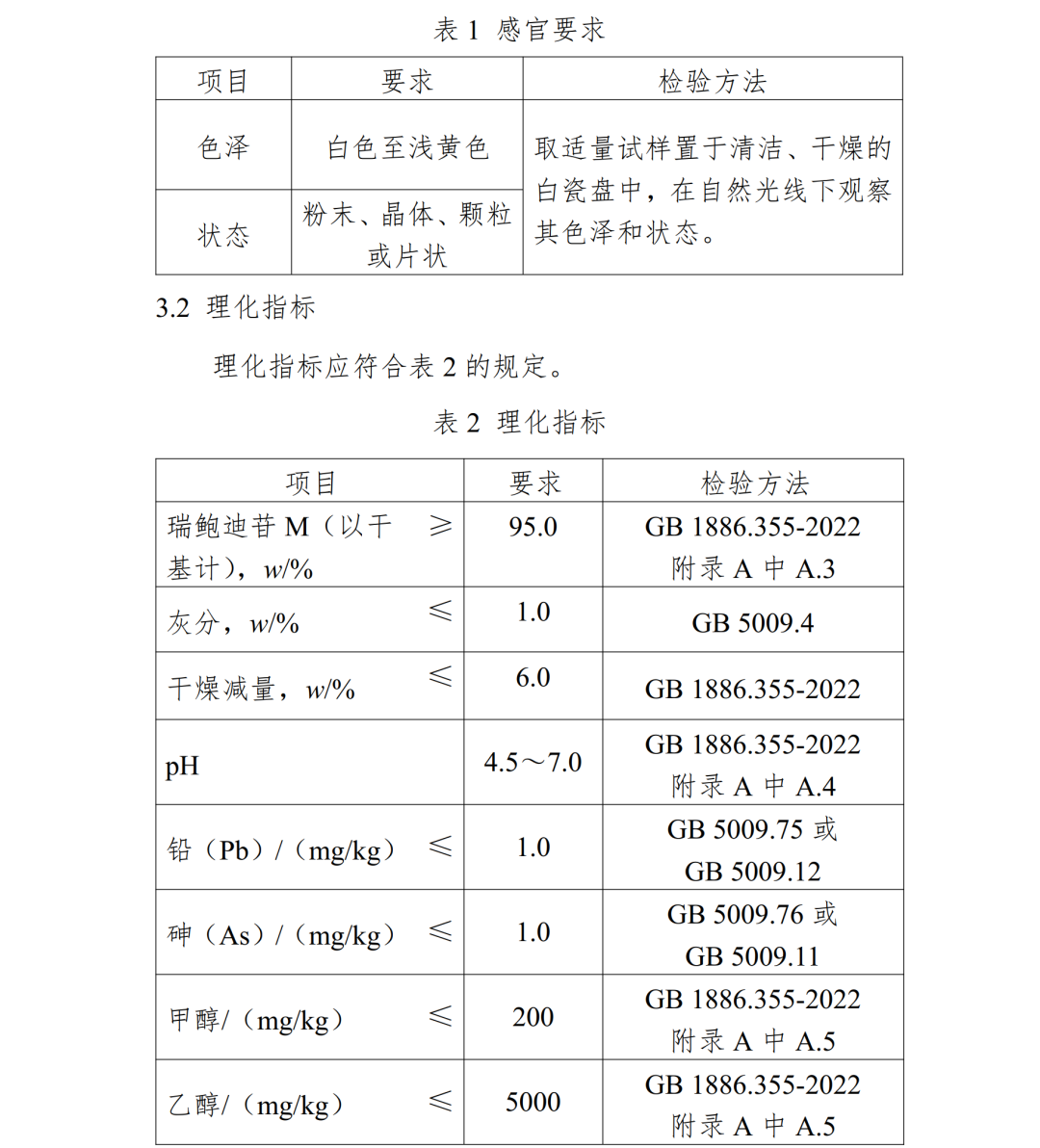


随后,卫健委于2025年第1号公告中批准其扩项。更新后的使用范围和使用量与GB 2760及相关公告中已批准的甜菊糖苷保持一致,允许单独或混合使用。


🪙欧盟
在Regulation (EC) No 1333/2008中,甜叶菊糖苷已被批准作为甜味剂用于食品添加(E编号为E 960:Steviol glycosides from Stevia (E 960a), Enzymatically produced steviol glycosides (E 960 c), Glucosylated steviol glycosides (E 960d)。

欧盟食品安全局(EFSA)亦对部分高纯度瑞鲍迪苷(如Reb A、Reb D、Reb M)进行了个别评估。Reb M的使用受到EFSA认可,并作为甜叶菊提取物的一部分纳入欧盟法规。
🗽美国
截至发稿日,美国FDA公认安全物质清单(GRAS Substances Inventories)中共有53例瑞鲍迪苷相关记录:其中2例正在安评(pending)阶段;1例应申请人要求停止评估(撤回)(At the notifier's request, FDA ceased to evaluate this notice);其余50例均收到FDA无异议回函.


国际法规状态
GRN 1206的通过,虽然并非Rebaudioside M首次获得FDA GRAS确认,但却具有特别的意义——这是由中国弈柯糖生物科技(上海)有限公司提交并获批的GRAS通告,标志着中国在天然高端甜味剂产业的国际化过程中迈出了坚实的一步。
截至目前,美国FDA已陆续通过了多个涉及甜菊糖苷(Steviol Glycosides)及其主要成分(如Reb A、Reb D、Reb M等)的GRAS通知,反映出该类别甜味剂在美国市场的成熟应用。然而,过去大多数GRAS通告的申请主体为欧美或日资企业,而GRN 1206的获批,代表着中国技术和中国企业在国际食品法规体系中赢得了高度认可。
未来,随着全球市场对低糖、天然、健康食品需求的持续增长,中国企业有望以技术创新和合规能力为支撑,在天然甜味剂领域赢得更多主动权并扩大国际市场份额。
鉴于全球食品原料创新趋势和监管要求不断演变,下周四(6 月 26 日),我们将在 CPHI2025 展会期间重磅举办《从中国到全球:2025 食品原料创新 & 合规论坛》。本次论坛特邀官方、协会、院校专家莅临现场,以前沿视角深度剖析法规政策走向与全球市场发展趋势,为行业同仁带来兼具前瞻性与实操价值的专业分享。
💡 重要提醒:免费注册通道仅剩 1 天关闭! 席位有限,诚邀您即刻锁定参会名额,共探食品原料领域的创新机遇与合规路径!现场还可免费领取“新食品原料全球市场准入指南”和抽奖!感兴趣不要错过~

🔥预见 2030:保健食品未来五年发展及合规趋势探讨(公益培训)

