2025年12月15日,WTO收到美国提交的关于“修订非处方药专论M020:非处方人用防晒药品”通知。此次修订拟将双-乙基己氧苯酚甲氧苯基三嗪添加为防晒活性成分,最高浓度达6%。意见征集时间为2025年12月12日至2026年1月26日。
01
美国防晒产品监管
美国将防晒产品作为药品进行监管。如符合相应非处方药(OTC)专论的要求,则不需要美国食品药品监管局(FDA)批准即可投放市场,但应按要求进行通报。如使用了未被收录在专论中的防晒剂,则作为新药管理,需要经FDA审查批准方可投放市场。美国联邦法规第352.10条及非处方药(OTC)专论M020列明了16种可接受的防晒剂及其最大允许使用浓度。
02
修订背景
Bemotrizinol(中文名称:双-乙基己氧苯酚甲氧苯基三嗪,INCI名称:Bis-Ethylhexyloxyphenol Methoxyphenyl Triazine),是一种有机紫外线(UV)过滤剂,具有高光稳定性,并能覆盖UVB(280-320nm)和 UVA(320-400nm)波段的广谱紫外线。
目前,含有双-乙基己氧苯酚甲氧苯基三嗪的药品在美国尚属非法销售。美国食品药品监督管理局(FDA)尚未批准任何以双-乙基己氧苯酚甲氧苯基三嗪为活性成分的药品上市申请,且目前该成分也未被列入任何非处方药专论的活性成分清单。
2024年9月23日,DSM公司根据《联邦食品、药品和化妆品法案》第505G(b)(5)条提交了一份一级非处方药专论申请OMOR,旨在申请批准双-乙基己氧苯酚甲氧苯基三嗪作为新的防晒成分,最高添加量为6%。在提交OMOR之前,申请人曾与FDA就该成分的OTC专论药物开发项目举行过正式会议。
2024年12月4日,美国食品药品监督管理局(FDA)认为该OMOR:(1)内容完整且格式正确,足以进行实质性审查;(2)包含足够的信息,可以证明含双-乙基己氧苯酚甲氧苯基三嗪的非处方药销售和使用是安全的。
2025年12月12日,为响应该申请,FDA在其网站上发布了题为“修订非处方药专论M020:非处方人用防晒药品”的拟议行政命令(拟议命令)(OTC000039)。FDA根据申请人提交的OMOR数据,对非临床、临床药理学以及临床安全性研究及信息进行审查,初步得出结论,有充分证据表明浓度高达6%的双-乙基己氧苯酚甲氧苯基三嗪可作为OTC防晒产品中的活性成分,用于6个月及以上成人和儿童是安全的。
03
修订内容
FDA发布了拟议行政命令(OTC000039),如果最终确定,该命令将对OTC专论M020进行修订。其中涉及双-乙基己氧苯酚甲氧苯基三嗪的内容主要包括:
1.新增防晒剂双-乙基己氧苯酚甲氧苯基三嗪,含量不超过6%;
2.双-乙基己氧苯酚甲氧苯基三嗪可与M020.10中防晒剂成分组合使用,但注意不得与对氨基苯甲酸(PABA)、三乙醇胺水杨酸盐(Trolamine salicylate)组合使用。
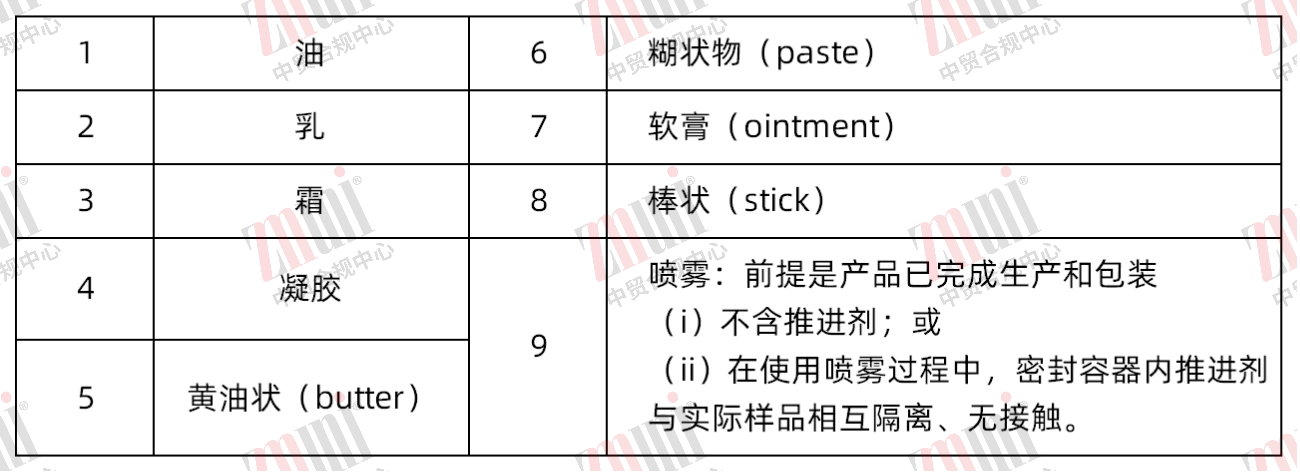
3.新增“M020.40 剂型”模块,产品剂型要求:
(a)如果防晒产品含有OTC专论M016中§M016.20 (e)列明的皮肤保护剂活性成分(例如尿囊素、聚二甲基硅氧烷、羊毛脂等),则需符合下表所列剂型;
(b)如果产品含有双-乙基己氧苯酚甲氧苯基三嗪防晒活性成分,则需满足§M020.40所列剂型;
04
写在最后
如果本拟议命令(OTC000039)最终生效,双-乙基己氧苯酚甲氧苯基三嗪将作为防晒活性成分被纳入OTC专论M020:非处方人用防晒药品,其最高添加量为6%。含有双-乙基己氧苯酚甲氧苯基三嗪的防晒产品,如果符合拟修订的OTC专论M020中相关条件,该产品则通常被认为是安全且有效的(GRASE),即不需再进行新药审批,按要求进行通报即可进入美国市场。
ZMUni中贸合规中心提醒您:双-乙基己氧苯酚甲氧苯基三嗪在国内做为准用防晒剂成分正常使用,但在本拟议命令(OTC000039)最终生效之前,如果出口美国的防晒产品含该成分,均按新药管理,需要经FDA审查批准方可投放市场。
