NMN作为当下食品行业的焦点原料,其全球合规之路一直牵动行业神经。2025 年 8 月,🔎我们曾对比解析过它在全球主要市场的监管现状;而今,伴随 12 月美国、澳大利亚两地 NMN 审批动态的更新,本文将为大家系统复盘其全球监管最新进展。
1.NMN在食品领域的全球监管现状一览(2025年12月)
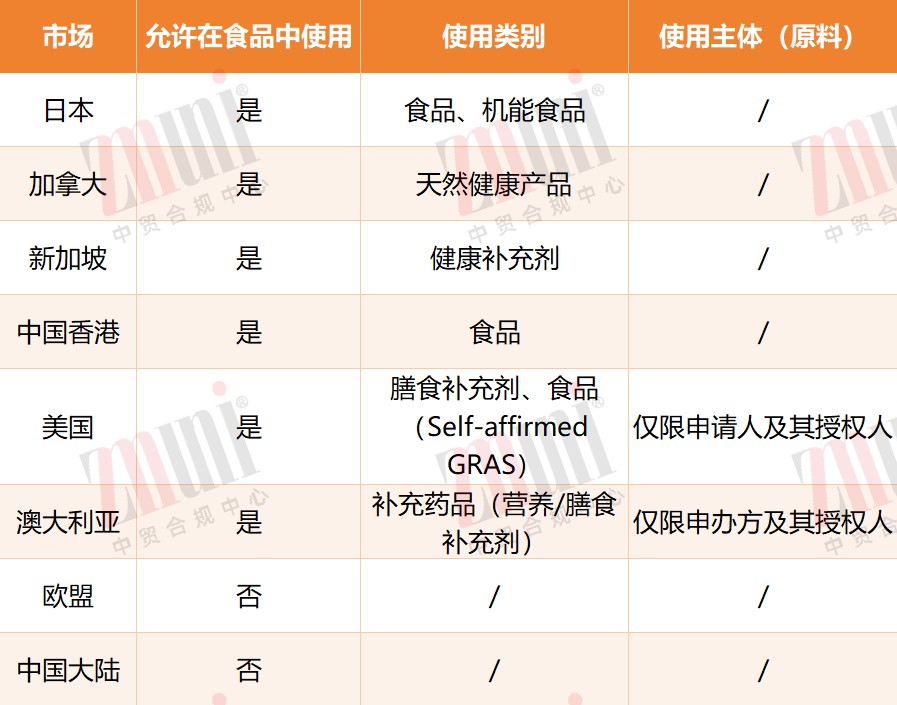
2. NMN在食品领域的全球合规进展介绍
3.总结
虽然各国对NMN准入门槛和监管态度呈现明显差异,但监管关注的核心角度相通。随着NMN在美国恢复新膳食成分(NDI)身份,在澳大利亚获准用于补充药品,欧盟亦推进相关安全性评估,加之其安全性与有效性研究的持续积累与深入推进,NMN在经历了一系列合规挑战与监管波折后,其合法身份正逐步趋于清晰。未来,NMN有望迎来国际市场合规发展的相对坦途,并为相关食品原料企业及跨境进口产品带来新的发展机遇。
如您需要NMN在国内外食品申报的相关合规协助,欢迎联系我们。
